病に苦しむ世界中の
患者さんを助ける。
HGFにはその可能性があります。
私たちについて
HGFタンパク質で
難病に苦しむ患者さんに対して
画期的な治療手段を提供する。
クリングルファーマは、レイトステージ(臨床試験後期の段階)の再生創薬バイオベンチャーです。現在、希少疾患を中心とする複数の難治性疾患を対象に、再生創薬シーズであるHGFタンパク質の 臨床試験を実施しています。

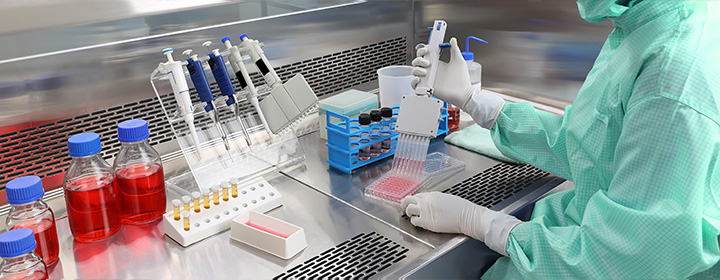
研究開発
HGF再生治療薬のプラットフォーマー
HGFはマルチな作用を持つ生体内タンパク質であり、組織や臓器を保護し、再生・修復する働きがあります。当社の強みは、HGFタンパク質を医薬品グレードで製造する体制を確立していることです。これをプラットフォームとし、難治性疾患治療薬の開発を推進しています。
企業情報
COMPANY
ニュース
NEWS